Система оценивания экзаменационной работы по химии
За правильный ответ на каждое из заданий 1-8, 12-16, 20, 21, 27-29 ставиться 1 балл.
Задания 9–11, 17–19, 22–26 считаются выполненными верно, если правильно указана последовательность цифр. За полный правильный ответ в заданиях 9–11, 17–19, 22–26 ставится 2 балла; если допущена одна ошибка – 1 балл; за неверный ответ (более одной ошибки) или его отсутствие – 0 баллов.
Теория по заданию:
- Тема №7 «Свойства простых веществ — металлов»
- Тема №8 «Свойства простых веществ — неметаллов»
- Тема №9 «Свойства соединений неметаллов»
- Тема №10 «Характерные химические свойства основных, амфотерных и кислотных оксидов»
- Тема №11 «Свойства оснований, амфотерных гидроксидов и кислот»
- Тема №12 «Соли»
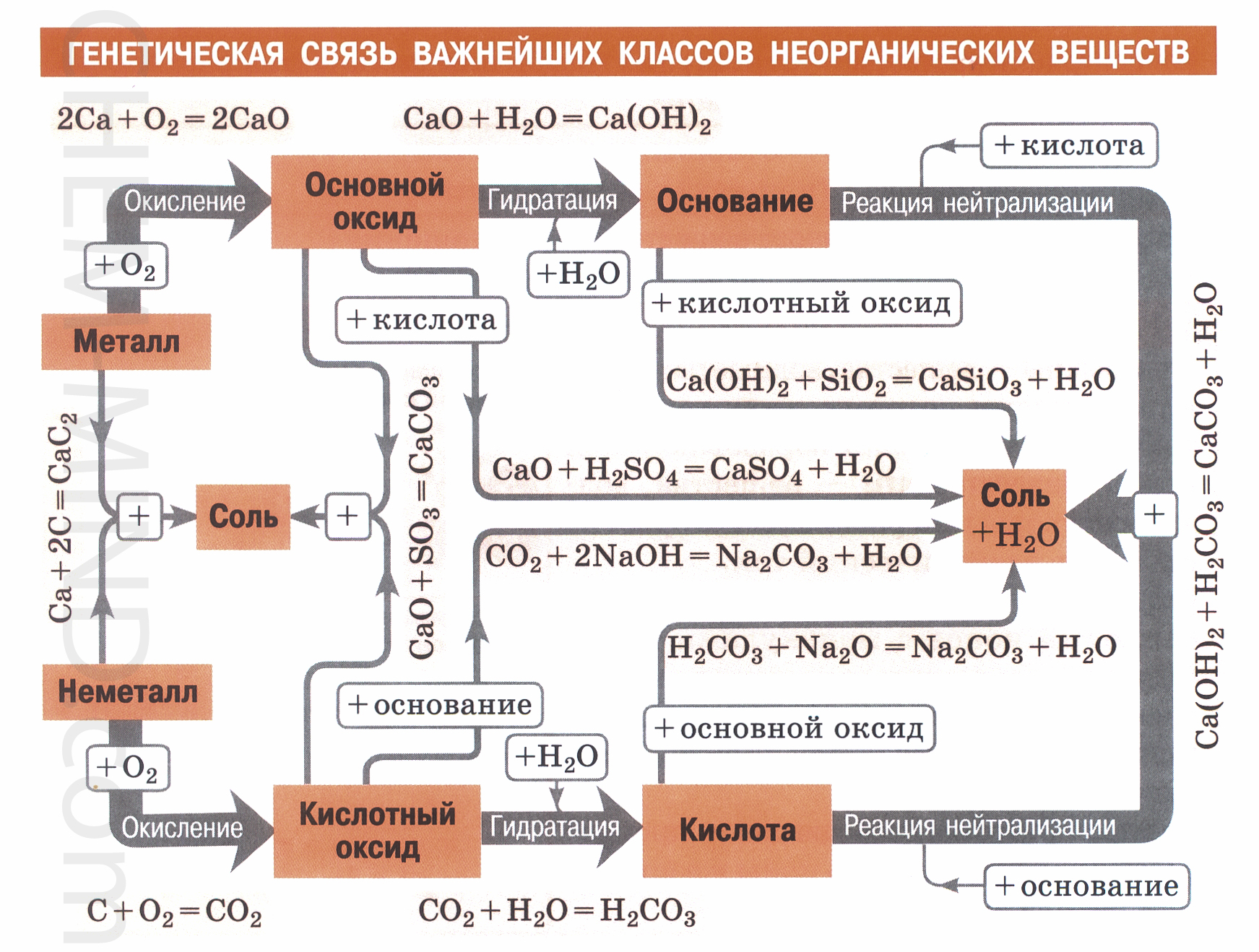
- Тема №13 «Взаимосвязь неорганических веществ»
Тест по заданию:
Задана следующая схема превращений веществ:
| +O2(изб.) | +H2 | |||
| ZnS | → | X | → | Y |
Определите, какие из указанных веществ являются веществами X и Y.
- Zn
- ZnO
- ZnH2
- Zn(OH)2
- ZnSO4
Задана следующая схема превращений веществ:
| X | ||||||
| ZnO | → | Zn | → | Y | → | Zn(OH)2 |
Определите, какие из указанных веществ являются веществами X и Y.
- CO2
- ZnCl2
- ZnS
- Zn3(PO4)2
- H2
Задана следующая схема превращений веществ:
| X | Y | |||
| Fe2O3 | → | Fe | → | FeSO4 |
Определите, какие из указанных веществ являются веществами X и Y.
- H2SO4(конц.)
- C
- H2SO4(разб.)
- SO2
- Al2(SO4)3
Задана следующая схема превращений веществ:
| FeO | → | X | → | Y | → | Fe(OH)3 |
Определите, какие из указанных веществ являются веществами X и Y.
- FeCl3
- FeCO3
- FeCl2
- FeS
- FePO4
Задана следующая схема превращений веществ:
| +Al | +H2SO4(разб.) | |||
| Fe2O3 | → | X | → | Y |
Определите, какие из указанных веществ являются веществами X и Y.
- Сульфат железа(II)
- Сульфит железа(III)
- Сульфат железа(III)
- Сульфид железа(II)
- Железо