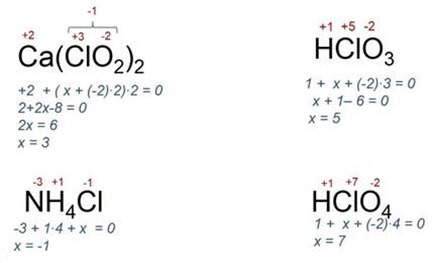Система оценивания экзаменационной работы по химии
За правильный ответ на каждое из заданий 1-8, 12-16, 20, 21, 27-29 ставиться 1 балл.
Задания 9–11, 17–19, 22–26 считаются выполненными верно, если правильно указана последовательность цифр. За полный правильный ответ в заданиях 9–11, 17–19, 22–26 ставится 2 балла; если допущена одна ошибка – 1 балл; за неверный ответ (более одной ошибки) или его отсутствие – 0 баллов.
Теория по заданию:
Тест по заданию:
Установите соответствие между уравнением реакции и изменением степени окисления окислителя в данной реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ |
| A) SO2 + NO2 = SO3 + NO | 1) –1 → 0 |
| Б) 2NH3 + 2Na = 2NaNH2 + H2 | 2) 0 → –2 |
| B) 4NO2 + O2 + 2H2O = 4HNO3 | 3) +4 → +2 |
| Г) 4NH3 + 6NO = 5N2 + 6H2O | 4) +1 → 0 |
| 5) +2 → 0 | |
| 6) 0 → –1 |
Установите соответствие между изменением степени окисления хлора в реакции и формулами веществ, которые вступают в эту реакцию: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ | ФОРМУЛЫ ИСХОДНЫХ ВЕЩЕСТВ |
| A) Cl0 → Cl–1 | 1) KClO3 (нагревание) |
| Б) Cl–1 → Cl0 | 2) Cl2 и NaOH (гор. р-р) |
| B) Cl+5 → Cl–1 | 3) KCl и H2SO4 (конц.) |
| Г) Cl0 → Cl+5 | 4) HCl и MnO2 |
| 5) KCl и O2 | |
| 6) KClO4 и H2SO4 (конц.) |
Установите соответствие между уравнением реакции и формулой вещества, которое в данной реакции является окислителем: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | ФОРМУЛА ОКИСЛИТЕЛЯ |
| A) H2S + I2 = S + 2HI | 1) NO2 |
| Б) 2S + C = CS2 | 2) H2S |
| B) 2SO3 + 2KI = I2 + SO2 + K2SO4 | 3) HI |
| Г) S + 3NO2 = SO3 + 3NO | 4) S |
| 5) SO3 | |
| 6) I2 |
Установите соответствие между уравнением окислительно-восстановительной реакции и свойством хлора, которое он проявляет в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | СВОЙСТВО ХЛОРА |
| A) Cl2 + 2NaOH = NaCl + NaClO + H2O | 1) является окислителем |
| Б) 2Fe + 3Cl2 = 2FeCl3 | 2) является восстановителем |
| B) 2NaCl + H2SO4(конц.) = Na2SO4 + 2HCl | 3) является и окислителем, и восстановителем |
| Г) 4HCl + O2 = 2H2O + 2Cl2 | 4) не проявляет окислительно-восстановительных свойств |
Установите соответствие между веществами, вступившими в реакцию, и степенью окисления азота в продукте: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | СТЕПЕНЬ ОКИСЛЕНИЯ АЗОТА |
| A) NH3 + O2 |
1) 0 |
| Б) NH3 + O2 |
2) +5 |
| B) NO2 + O2 + H2O → | 3) +3 |
| Г) NH3 + CuO |
4) +2 |
| 5) –2 |